Теоретические основы кинетики биохимической очистки
Определить порядок реакции биохимической очистки можно графическим методом. Для этого необходимо экспериментально измерить изменение концентрации одного из реагентов в различные моменты времени, т.е С1 (τ1); С2 (τ 2); .;Сn (τ n). Первым этапом исследования является определение целочисленного значения порядка реакции. Из уравнений (4.7) и (4.8) следуют зависимости для нулевого, первого, второго и третьего порядков реакции:
= 0; ![]() ; (4.9)= 1;
; (4.9)= 1; ![]() ; (4.10)= 2;
; (4.10)= 2; ![]() (4.11)= 3;
(4.11)= 3; ![]() (4.12)
(4.12)
Из полученных уравнений (4.9) - (4.12) следуют линейные зависимости в функциональных координатах, присущих определенному порядку реакции:
= 0; ![]() ; (4.13)= 1;
; (4.13)= 1; ![]() (4.14)= 2;
(4.14)= 2; ![]() (4.15)= 3;
(4.15)= 3; ![]() (4.16)
(4.16)
Опытные данные последовательно изображают в функциональных координатах (4.12) - (4.16) до тех пор, пока не будет обнаружена линейная зависимость, которой и соответствует порядок реакции. В нашем случае линейная зависимость наблюдается при использовании уравнения соответствующего первому порядку реакции.
На скорость биохимических реакций существенное влияние оказывает температура. Это влияние, предварительно вычислив энергию активации, можно вычислить с помощью уравнения Аррениуса
![]() (4.17)
(4.17)
где k0 - предэкспоненциальный множитель; Е - энергия активации; R - универсальная газовая постоянная; Т - температура, К. Константы уравнения Е и k0 не зависят (или мало зависят) от температуры.
Для обоснования уравнения (4.17) Я. Вант-Гофф и С. Аррениус ввели понятие энергетического барьера, который необходимо преодолеть участникам реакции. Величина этого барьера характеризуется той минимальной избыточной энергией Е (по сравнению со средней величиной), которой должны обладать реагирующие вещества для того, чтобы произошла реакция.
Зная энергию активации, можно рассчитать константу скорости реакции (К2) при температуре Т2, если она известна при температуре Т1. Логарифмируя уравнение (4.17) при двух температурах и учитывая, что Е и k0 не зависят от температуры, получаем
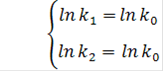 (4.18)
(4.18)
Решение системы (4.18) позволяет найти Е и k0.
Теоретическое обоснование уравнения Аррениуса дала теория переходного состояния Эйринга и Поляни. Основное уравнение этой теории раскрывает смысл энергии активации и предэкспоненциального множителя.
![]() (4.19)
(4.19)
Где ![]() =6,02∙1023 - число Авогадро; h=6,625∙10-34 Дж∙с - постоянная Планка;
=6,02∙1023 - число Авогадро; h=6,625∙10-34 Дж∙с - постоянная Планка; ![]() - энтропия образования переходного состояния;
- энтропия образования переходного состояния; ![]() - энтальпия образования переходного состоянии, равная энергии активации.
- энтальпия образования переходного состоянии, равная энергии активации.
Еще статьи по теме
Расчет и анализ показателей экономической эффективности строительного производства
Капитальное
строительство - одно из важнейших отраслей материального производства.
Назначение капитального строительства состоит в том, что оно обеспечивает все
отрасли народного хозяйства - промышленность, сельское хозяйство, транспорт,
...
Понятие и значение водных ресурсов
Вода
- ценнейший природный ресурс. Она играет исключительную роль в процессах обмена
веществ, составляющих основу жизни. Огромное значение вода имеет в промышленном
и сельскохозяйственном производстве. Общеизвестна необходимость ее для быт ...